Setticemia neonatale nel cane e nel gatto
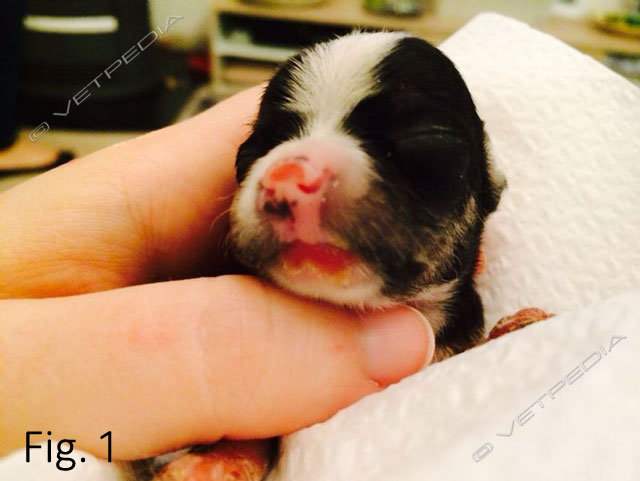
Nel cane e nel gatto il tasso di mortalità perinatale è altamente variabile e comprende i decessi che avvengono durante il parto, immediatamente dopo la nascita e durante il periodo neonatale, compreso tra la nascita e il compimeAnto della quarta settimana di età. Ancor più che in altre specie animali, in queste due specie il periodo neon...
Self-Assessment Colour Review - Chirurgia 1
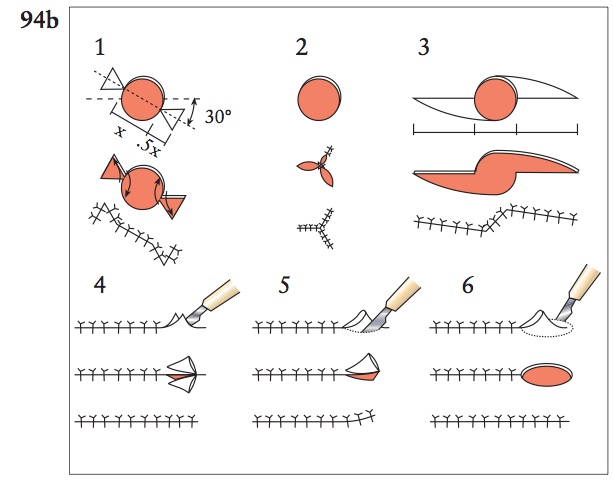
La ferita illustrata (94a) è quanto residua dopo asportazione di un mastocitoma in un cane. La cute a disposizione per chiudere il difetto è abbondante. i. Nomina le tre tecniche di sutura che possono essere utilizzate per riparare questa ferita circolare. ii. La prima sutura ha determinato la formazione di un “orecchio di cane”. Elenca...
Una passione secolare: lo scalare nell’acquario d’acqua dolce tropicale
Pterophyllum scalare (Schultze, 1823) è una delle specie più diffuse e amate nell’acquariofilia tropicale d’acqua dolce. Sulla cresta dell’onda da più di un secolo, la specie è oggi ampiamente disponibile in tutti i negozi del settore con numerose varietà, conseguenza frutto di una secolare selezione zootecnica e di una costante richiesta...
Ectoparassitosi del criceto
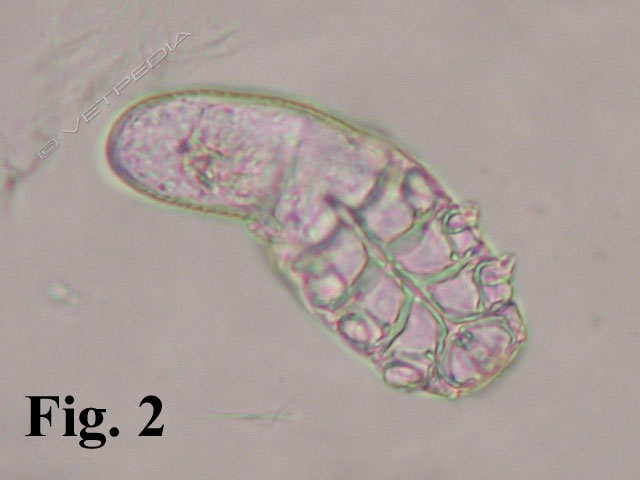
Nel criceto è abbastanza comune la demodicosi, che può essere sostenuta da due specie, Demodex criceti e Demodex aurati. Entrambi gli acari sono normali residenti della cute del criceto, e la forma clinica si osserva di solito in animali malnutriti, anziani e/o immunodepressi. Si osserva alopecia, eritema, scaglie e croste, ma in genere n...
Ipertiroidismo felino: Test di soppressione con T3
Il test di soppressione con T3 è il test dinamico di valutazione della funzionalità tiroidea più sicuro ed affidabile a disposizione per la specie felina. L’obiettivo del test è quello di dimostrare nei soggetti non affetti da ipertiroidismo la presenza di un feed-back negativo sulla produzione di ormoni tiroidei dopo somministrazione eso...
Avvelenamento da rodenticidi anticoagulanti
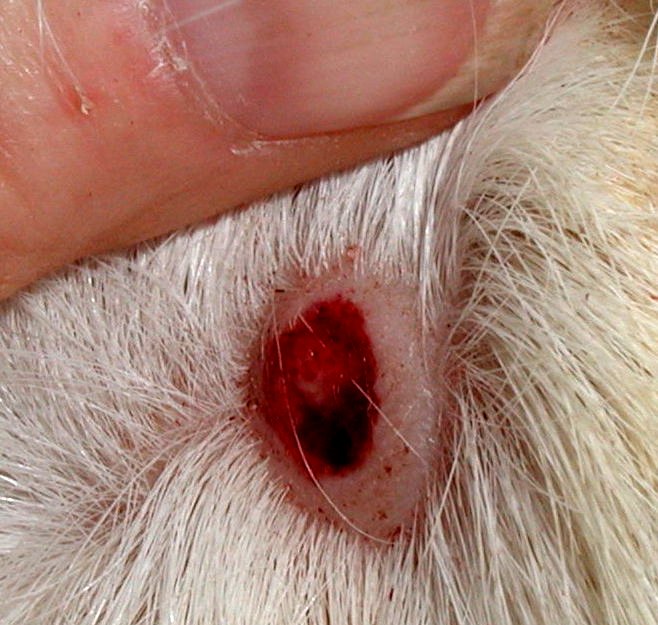
Nel 1940 una piccola industria farmaceutica inglese suggerì che il dicumarolo potesse avere attività rodenticida. Negli anni successivi gli studi confermarono questa ipotesi e subito dopo la Seconda Guerra Mondiale il primo rodenticida anticoagulante, il warfarin, venne messo in commercio e ampiamente utilizzato in molti Paesi. L’ingestio...
Alimentazione delle tartarughe
Le tartarughe andrebbero nutrite nel modo più naturale possibile e con un'alimentazione quanto più vicina a quella che troverebbero nel loro habitat. Detto ciò possiamo dire che le tartarughe, dal punto di vista dell'alimentazione, si suddividono in erbivore, carnivore e onnivore. ALIMENTAZIONE ERBIVORATra le molte specie erbivore trovia...
Tumori cutanei della cavia
Nella cavia i tumori cutanei rappresentano il 15% di tutte le neoplasie. Il più comune tumore cutaneo è il tricofollicoloma, una neoplasia benigna delle cellule basali. Si localizza principalmente sul dorso e sui fianchi e può raggiungere dimensioni notevoli; appare come un nodulo sottocutaneo sodo, rotondeggiante. L’asportazione chirurgi...
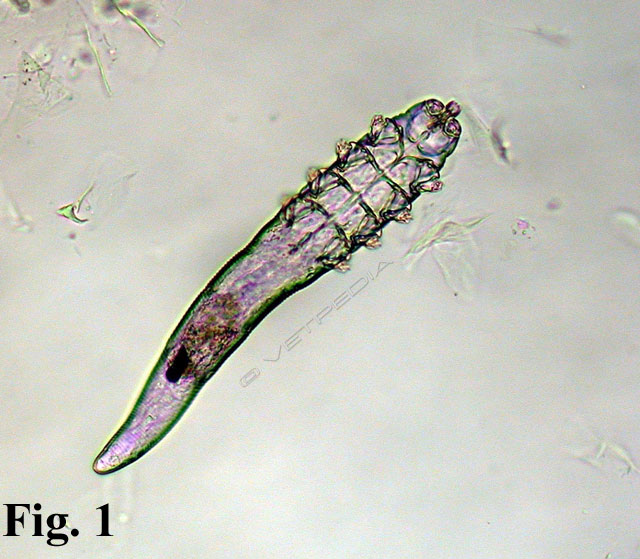
Demodicosi canina
La demodicosi canina, nota anche come rogna demodettica, è una malattia dermatologica molto frequente del cane, di origine parassitaria, non contagiosa e sostenuta da acari del genere Demodex. Nel cane sono riconosciute tre specie di acari: Demodex canis, responsabile della quasi totalità dei casi, Demodex cornei e Demodex injai, sebbene ...
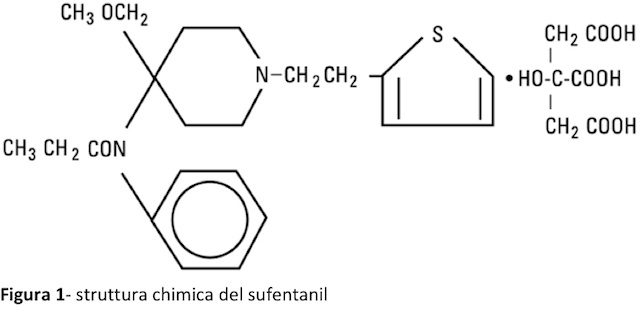
Sufentanil
Il sufentanil citrato, introdotto in anestesia umana negli anni ’70, è un oppioide agonista puro di sintesi, analogo tienilico del fentanyl (Fig. 1) più potente della morfina e caratterizzato da una durata d’azione relativamente breve.Diversi studi, condotti sia in vivo che in vitro, hanno evidenziato che il sufentanil ha una selettività ...